来源:生物世界 2025-12-04 14:34
肥胖患者的内脏脂肪组织(VAT)来源的细胞外囊泡(EV)促进胰腺癌的发展并使其对免疫检查点阻断(ICB)疗法产生耐药性。肥胖与多种癌症类型的发展有关,其中,患有胰腺导管腺癌(PDAC)的肥胖患者预后极差,且对检查点阻断(ICB)疗法具有耐药性。然而,其背后的分子机制在很大程度上仍不明确。
2025 年 12月2日,中山大学肿瘤防治中心林东昕院士、郑健研究员、黄旭东副研究员作为共同通讯作者(薛春玲、赵思涵、周一帆和陈子明为论文共同第一作者),在 Cell 子刊Cell Metabolism上发表了题为:Extracellular vesicles from obese visceral adipose promote pancreatic cancer development and resistance to immune checkpoint blockade therapy的研究论文。该研究首次发现,肥胖患者的内脏脂肪组织(VAT)来源的细胞外囊泡(EV)促进的发展并使其对免疫检查点阻断(ICB)疗法产生耐药性。

在这项最新研究中,研究团队发现,肥胖患者的内脏脂肪组织(VAT)能够通过传递携带信号分子的细胞外囊泡(EV)与远端胰腺导管腺癌(PDAC)组织进行信息交流。
研究团队揭示,胰腺导管腺癌(PDAC)细胞能够将 VAT-EV 吸收到其溶酶体中,在那里 EV 中携带的组织蛋白酶 A(Ctsa)稳定核糖核酸酶 Rnaset2b,产生大量游离的假尿苷(Pseudouridine)。假尿苷通过增加活性氧(ROS)并降低基因启动子处的 H3K27me3 修饰,从而激活肥大细胞(Mast Cell)。活化的肥大细胞抑制 CD8+T 细胞活性,形成免疫抑制性的肿瘤微环境,从而促进癌症进展。进一步动物实验表明,敲低 Ctsa,能够有效增强免疫检查点阻断(ICB)疗法对胰腺导管腺癌(PDAC)的治疗效果。
该研究的核心发现:
VAT-EV 及其所携带的 Ctsa 蛋白介导脂肪组织与肿瘤组织之间的器官间通讯;
VAT-EV 递送的 Ctsa 可稳定核糖核酸酶Rnaset2b 以生成游离的假尿苷;
假尿苷重塑染色质并导致肥大细胞活化;
靶向 VAT-EV-CTSA-假尿苷-肥大细胞信号可有效增强免疫检查点阻断疗法的疗效。
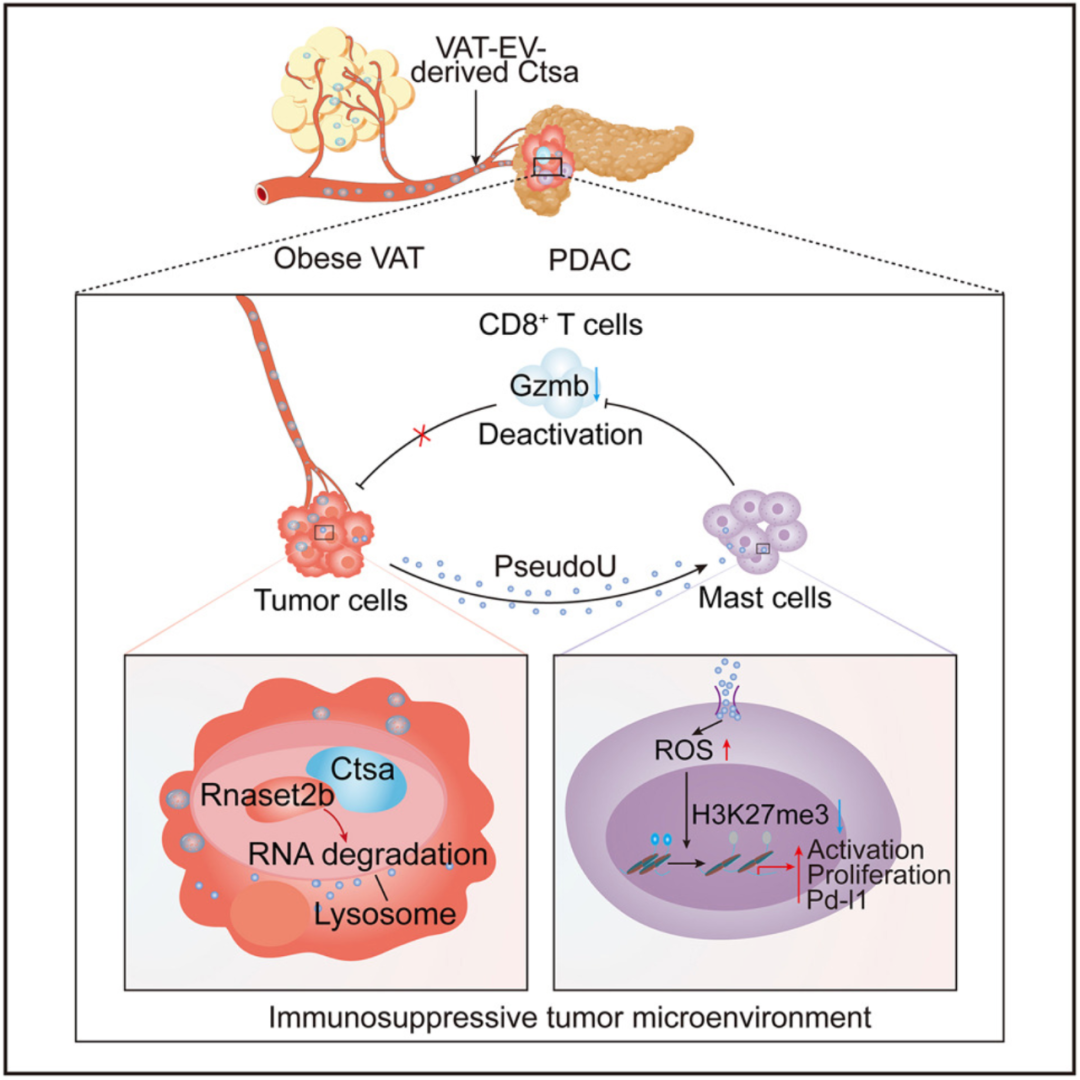
总的来说,该研究揭示了肥胖与癌症之间存在一个由 内脏脂肪组织-细胞外囊泡-CTSA-假尿嘧啶-肥大细胞 (VAT-EV-CTSA-Pseudouridine-Mast Cell)信号轴,为开发肥胖相关癌症的新治疗策略带来了希望。
论文链接:
https://www.cell.com/cell-metabolism/abstract/S1550-4131(25)00475-9
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->