海洋是地球上最大的活性碳库。海洋微生物在全球碳循环中发挥着重要作用。然而,由于大多数海洋微生物难以培养、其原位代谢功能难以测定等技术瓶颈,关于海洋微生物光合固碳的原位功能机制存在争议。
中国科学院青岛生物能源与过程研究所与英国牛津大学、英国谢菲尔德大学、山东海洋科学研究所等合作。并基于拉曼分选耦合单细胞基因组(scRACS-Seq)靶向CO2固定活性等仪器和手段,揭示了在海水中进行原位光合固碳的SAR11组,发现它们利用视紫红质作为光捕获系统来驱动海水中的CO2固定。近日,相关研究成果发表在《生物设计研究》(生物设计研究)上。
为了确定海洋微生物组中的哪些细胞可以原位固定CO2,由高级工程师荆晓燕、助理研究员龚延海和博士滕旭领导的研究小组用稳定同位素13C标记的无机碳底物喂养新鲜海水样品。通过单细胞拉曼光谱中类胡萝卜素等色素特征峰的红移现象,建立了无需培养即可原位固定CO2的单细胞的鉴定和测定流程。基于单细胞中心开发的scRACS-Seq系统,研究人员建立了针对CO2固定活性等代谢表型的单细胞功能靶向拉曼分选和测序方法。
利用scRACS-Seq系统,对山东青岛崂山湾透光层海水中的一系列浮游动物单细胞(来自SAR11和其他类群的浮游动物单细胞)进行了鉴定和分类。基于SAR11单细胞的全基因组序列(覆盖高达100%)的进化分析、基因功能预测和代谢途径重建,研究表明它们具有完整的类胡萝卜素合成途径,证实了上述单细胞拉曼光谱基于色素峰红移鉴定和表征CO2固定活性的原理。发现了一种基于光激活质子泵系统的蛋白视紫红质,包括双加氧酶、视紫红质光敏蛋白和F型ATP合酶等关键蛋白。它们具有卡尔文-本森循环途径中用于固定CO2的大部分基因。这些SAR11细胞可能通过基于视紫红质的光反应质子泵系统驱动基于卡尔文-本森循环的海水原位固碳。为了验证这一假设,在这些单细胞基因组中预测为视紫红质光敏蛋白的四个基因在大肠杆菌中异源表达.结果表明,它们能够合成视紫红质,其中的两个基因与GenBank中的基因没有明显的同源性,属于一类全新的视紫红质感光蛋白。因此,这些视紫红质介导的光活化质子泵系统或SAR11的能量引擎用于海水中的原位光合作用和碳隔离。
SAR11难以培养,缺乏研究工具。然而,这项研究以单细胞精度揭示了SAR11的代谢表型和完整基因组,从而建立了视紫红质光敏蛋白与海水原位CO2固定之间的功能关系。这一独创的拉曼介导靶向单细胞基因组(scRACS-Seq)仪器系统克服了当前拉曼介导靶向宏基因组方法通常难以在单个细菌细胞中获得高覆盖率基因组的瓶颈,因此对于环境中活体暗物质的功能探索和机制分析具有普遍的方法论意义。
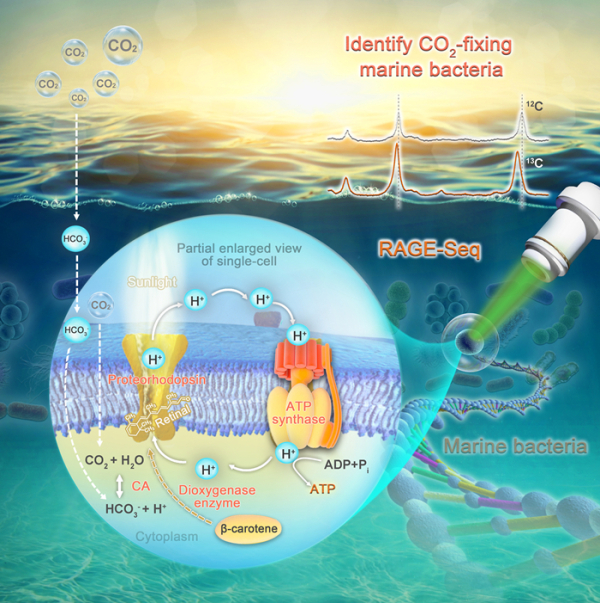
单细胞海洋微生物组的精确拉曼分选和测序技术(scRACS-Seq)